Nr 1 pod względem „pushability”⁴
O 96% większa siła przenoszona od złączki do końcówki.
Nr 1 pod względem „trackability”⁴
Przesuwanie w stronę zmiany wymaga użycia nawet o 33% mniejszej siły.
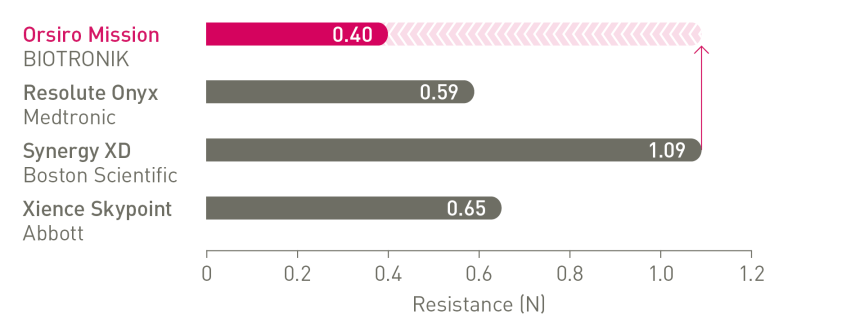
Nr 1 pod względem „crossability”⁴
Do przechodzenia przez trudne miejsca potrzeba użyć nawet o 64% mniej siły.