Suportes mais finos para baixa força externa crônica (COF)
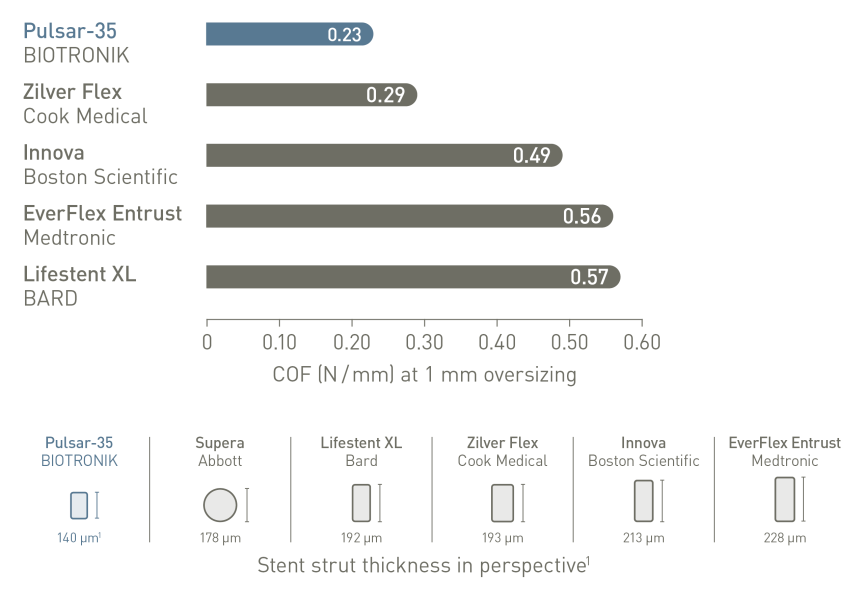
Hastes mais finas e menor COF fazem a diferença:
• Menor risco de reestenose;
• Redução de lesões e inflamação nos vasos;
• Endotelização mais rápida.
Indicado para o uso em pacientes com doença aterosclerótica das artérias femoral e poplítea proximal, e para o tratamento de resultados insuficientes após angioplastia transluminal percutânea (PTA), por exemplo, estenose residual e dissecção.*

• Menor risco de reestenose;
• Redução de lesões e inflamação nos vasos;
• Endotelização mais rápida.
Os resultados clínicos do Pulsar-18 podem ser usados para ilustrar os resultados clínicos do Pulsar-35 devido a plataformas de stent idênticas FTLR – Livre de revascularização da lesão-alvo; PP – Patência Primária; TODOS – Comprimento médio da lesão.
Força radial suficiente para um suporte do vaso a longo prazo, mesmo em lesões calcificadas.
| Stent | |
|---|---|
| Tipo de cateter | OTW |
| Fio guia recomendado | 0,035" |
| Material do stent | Nitinol |
| Espessura da haste | 140 μm |
| Largura da haste | 85 μm |
| Revestimento do stent | proBIO® (carbeto de silício amorfo) |
| Marcas no stent | 6 marcas de ouro em cada extremidade |
| Tamanhos | ø 5,0 - 7,0 mm; C: 30 - 200 mm |
| Shaft proximal | 6 F, revestimento hidrofóbico |
| Comprimento útil | 90 e 135 cm |
<
| ø do stent (mm) |
Comprimento do cateter 90 cm (Comprimento do stent mm) |
|||||||||
|---|---|---|---|---|---|---|---|---|---|---|
| 30 | 40 | 60 | 80 | 100 | 120 | 150 | 170 | 200 | ||
| 6F | 5 | 379878 | 379879 | 379880 | 379881 | 379917 | 379918 | 379919 | 379920 | 379921 |
| 6 | 379883 | 379884 | 379885 | 379886 | 379922 | 379923 | 379924 | 379925 | 379926 | |
| 7 | 379888 | 379889 | 379890 | 379891 | 379927 | 379928 | 379929 | 379930 | 379931 | |
| ø do stent (mm) |
Comprimento do cateter 135 cm (Comprimento do stent mm) |
|||||||||
|---|---|---|---|---|---|---|---|---|---|---|
| 30 | 40 | 60 | 80 | 100 | 120 | 150 | 170 | 200 | ||
| 6F | 5 | 379898 | 379899 | 379900 | 379901 | 379937 | 379938 | 379939 | 379940 | 379941 |
| 6 | 379903 | 379904 | 379905 | 379906 | 379942 | 379943 | 379944 | 379945 | 379946 | |
| 7 | 379908 | 379909 | 379910 | 379911 | 379947 | 379948 | 379949 | 379950 | 379951 | |
RLA = Revascularização da Lesão Alvo; ALL = Comprimento Médio da Lesão
1.Dados em arquivo da BIOTRONIK. Diâmetros de 6,0 mm; 2. Dados em arquivo da BIOTRONIK. Diâmetros de 6,0 mm. Não foi possível testar o stent Supera devido ao seu desenho e método de teste aplicado; 3. Zhao HQ Late stent expansion and neointimal proliferation of oversized nitinol stents in peripheral arteries. Cardiovasc. Interv. Radiol. 2009; 32(4); 720-6; 4. Koskinas C. Role of endothelial shear stress in stent restenosis and thrombosis: pathophysiologic mechanisms and implications for clinical translation. JACC 2012 10;59(15):1337-49; 5. Koppara T. Thrombogenicity and early vascular healing response in metallic biodegradable polymer-based and fully bioabsorbable drug-eluting stents. Circ Cardiovasc Interv. 2015 8(6):e002427; 6. Funovics M. Correlation between chronic outward force (COF) and neointimal hyperplasia in self-expanding nitinol stents in swine in clinically relevant oversizing ranges. Apresentado em: LINC, 26 de janeiro de 2017; Leipzig, Alemanha; 7. Lichtenberg et al. Effectiveness of the Pulsar-18 self-expanding stent with optional drug-coated balloon angioplasty in the treatment of femoropopliteal lesions - the BIOFLEX PEACE All-Comers Registry.Vasa (2019), 1-9. doi_10.10240301-1526a000785; 8.Bosiers M et al. 4-French - compatible endovascular material is safe & effective in the treatment of femoropopliteal occlusive disease: Results of the 4EVER Trial. ENDOVASC THER 2013; 20: 746-756; 9. Lichtenberg M. Superficial Femoral Artery TASC D registry: 12-month effectiveness analysis of the Pulsar-18 SE nitinol stent in patients with critical limb ischemia. J Cardiovasc Surg (Torino). 2013; 54(4):433-9; 10. Dados em arquivo da BIOTRONIK.
Os concorrentes líderes foram selecionados com base nas receitas de mercado de stents PV de 2017 (UE) e nas receitas de mercado de stents PV de 2015 (APAC); (Fonte:
Millennium Research Group Inc.).
*Indicação conforme o manual técnico. Pulsar e proBIO são marcas comerciais ou marcas registradas do grupo de empresas BIOTRONIK. Todas as outras marcas são propriedade dos seus respectivos proprietários.