Freesolveᵀᴹ
Indiziert zur Behandlung von De-Novo-Läsionen der Koronararteriena
Unterstützung
Resorbierbare Koronarscaffolds weiten verengte Koronararterien auf und bieten eine temporäre Gefäßunterstützung. Dadurch ermöglichen sie einen ungehinderten Blutfluss in den Koronararterien bei niedrigen Raten von Stentthrombose (ST) und Revaskularisierung der Zielläsion (TLR).
Resorption
Nachdem sie ihre stützende Funktion erfüllt haben, werden Scaffolds vom Körper resorbiert und bieten so volle Flexibilität bei zukünftigen Therapien.
Produkt-Highlights
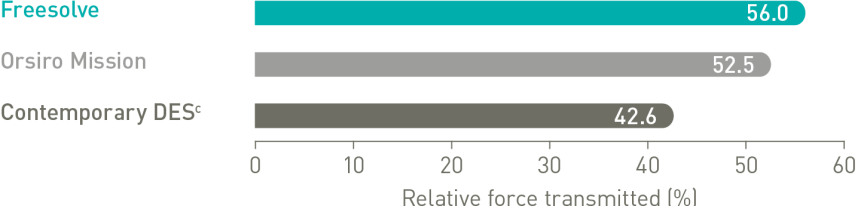
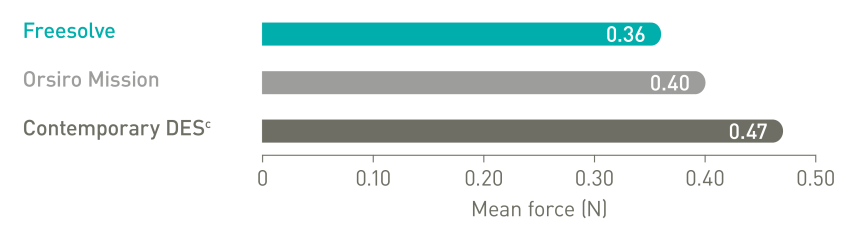
Platzierung wie bei einem DES5
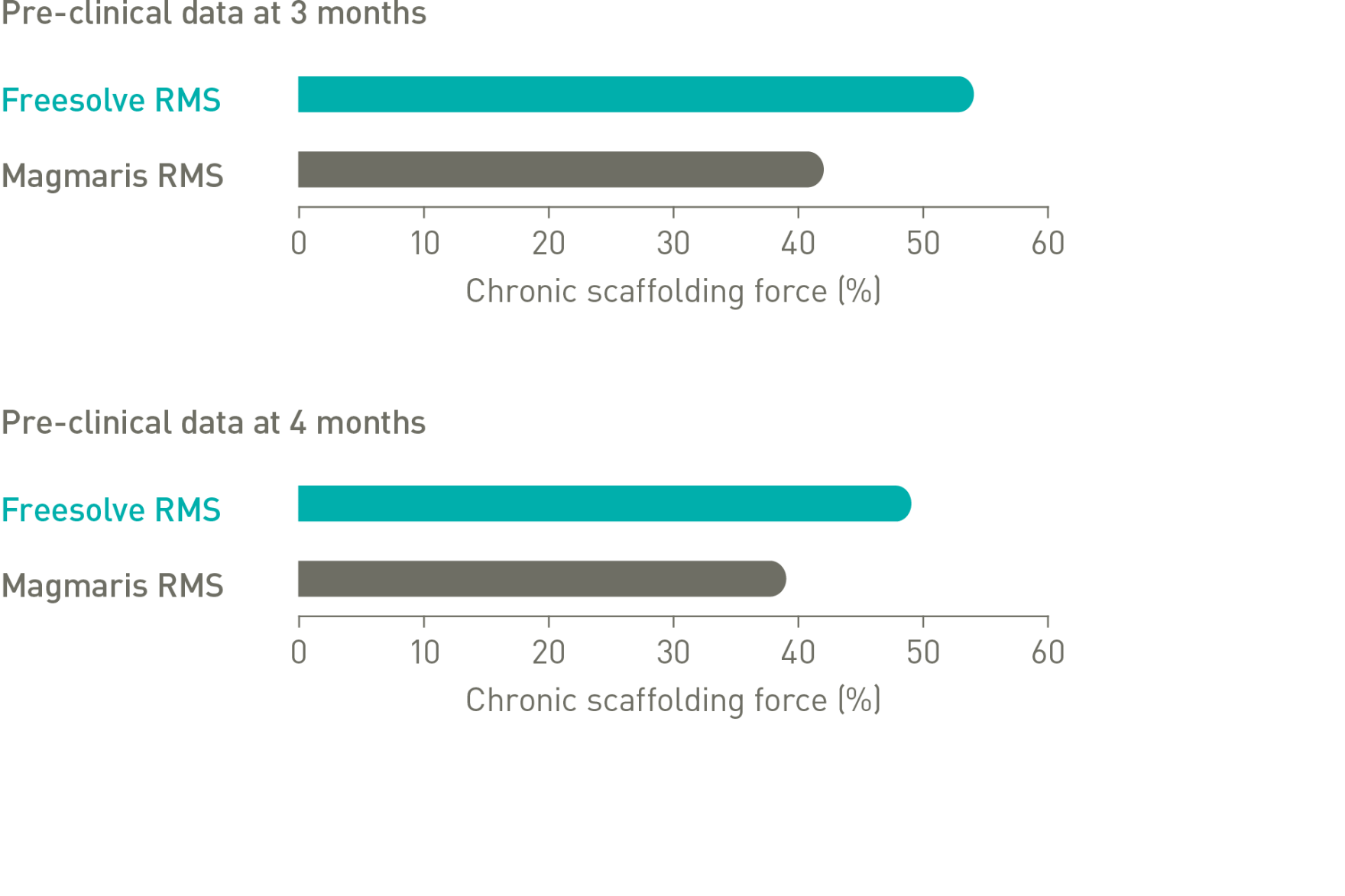
Optimale Gefäßunterstützung6,7
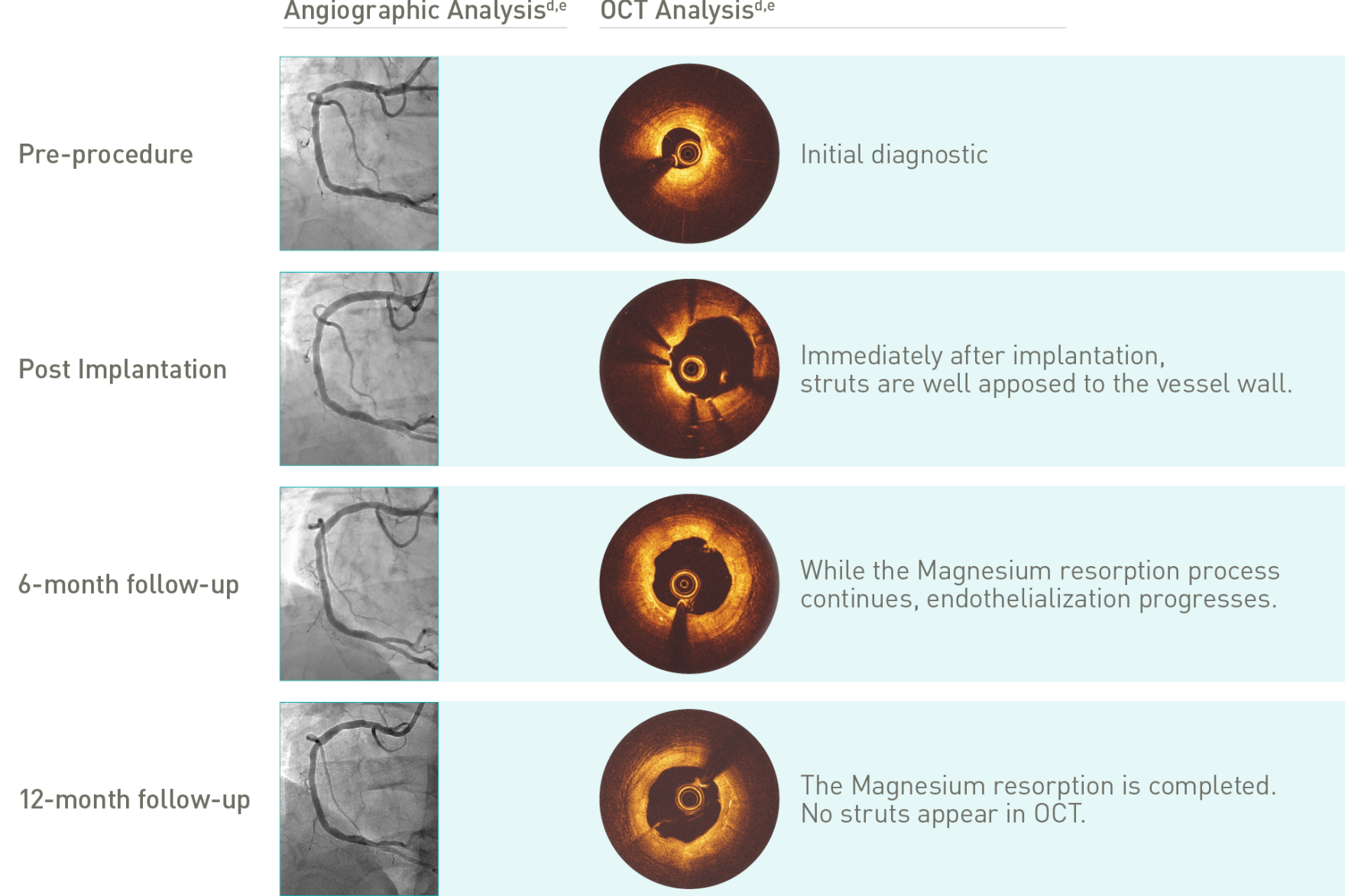
Magnesium nach 12 Monaten vollständig resorbiert8
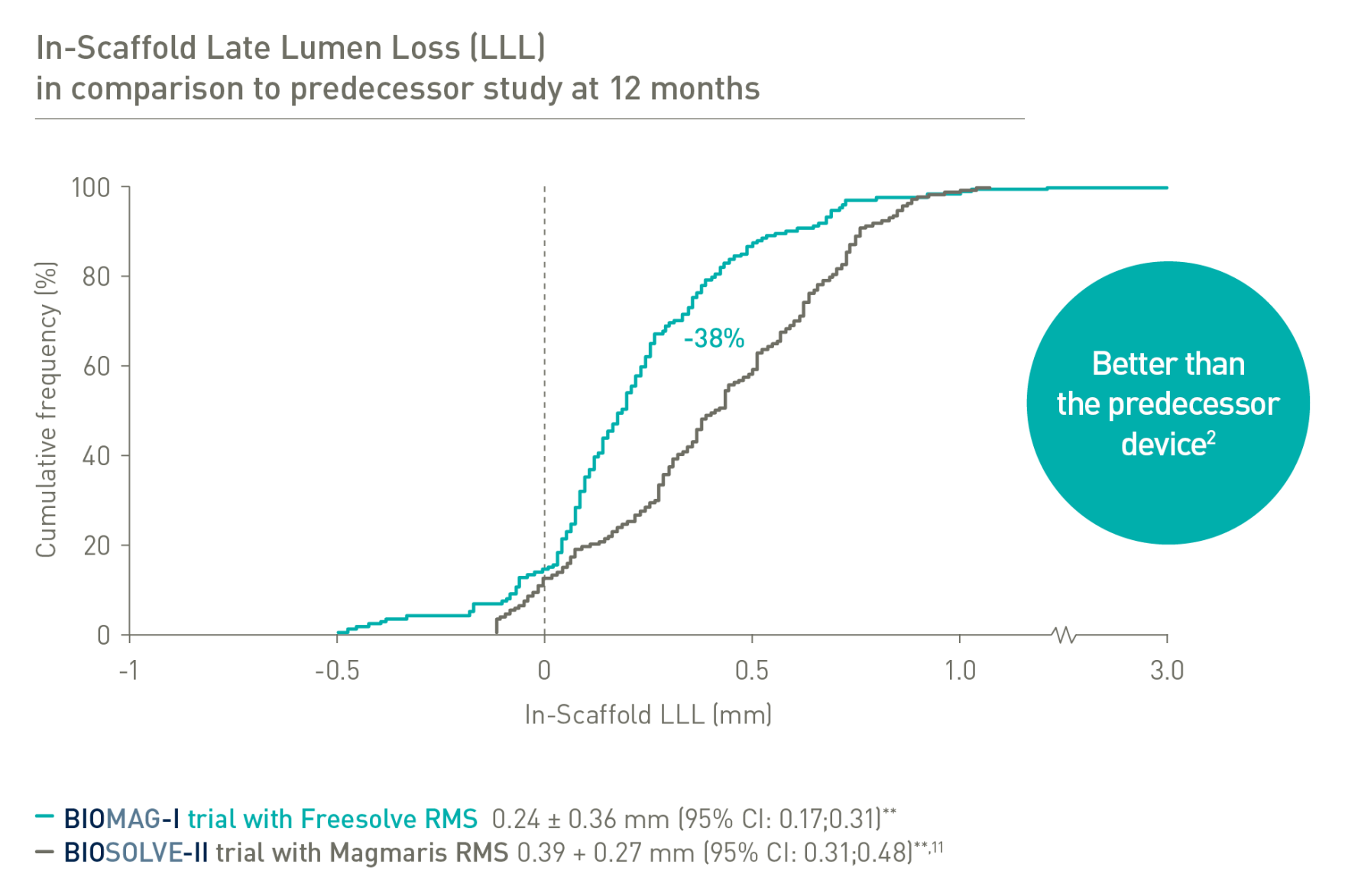
Hervorragende Sicherheit und Wirksamkeit2,3
Vorhersehbarer, gleichmäßiger Resorptionsprozess⁶
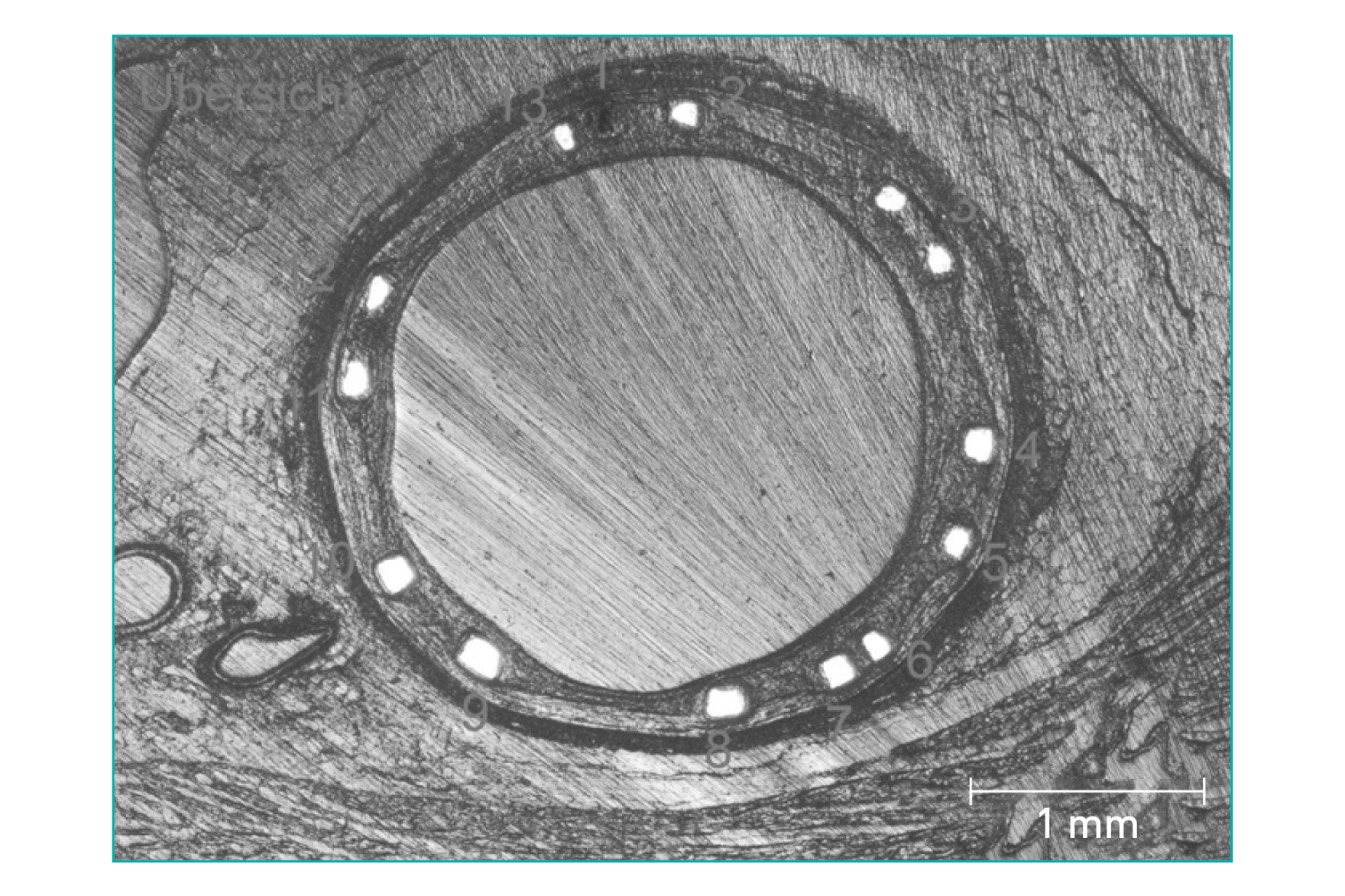
Gleichmäßige Resorption der Streben6
Gleichmäßige Form durch homogene Strebenresorption6
Mehr als 3 Monate Gefäßunterstützung6,7
> 99 % der Streben nach 12 Monaten nicht mehr sichtbar8
First-In-Human-Studie (FIH) BIOMAG-I3
Produktüberblick
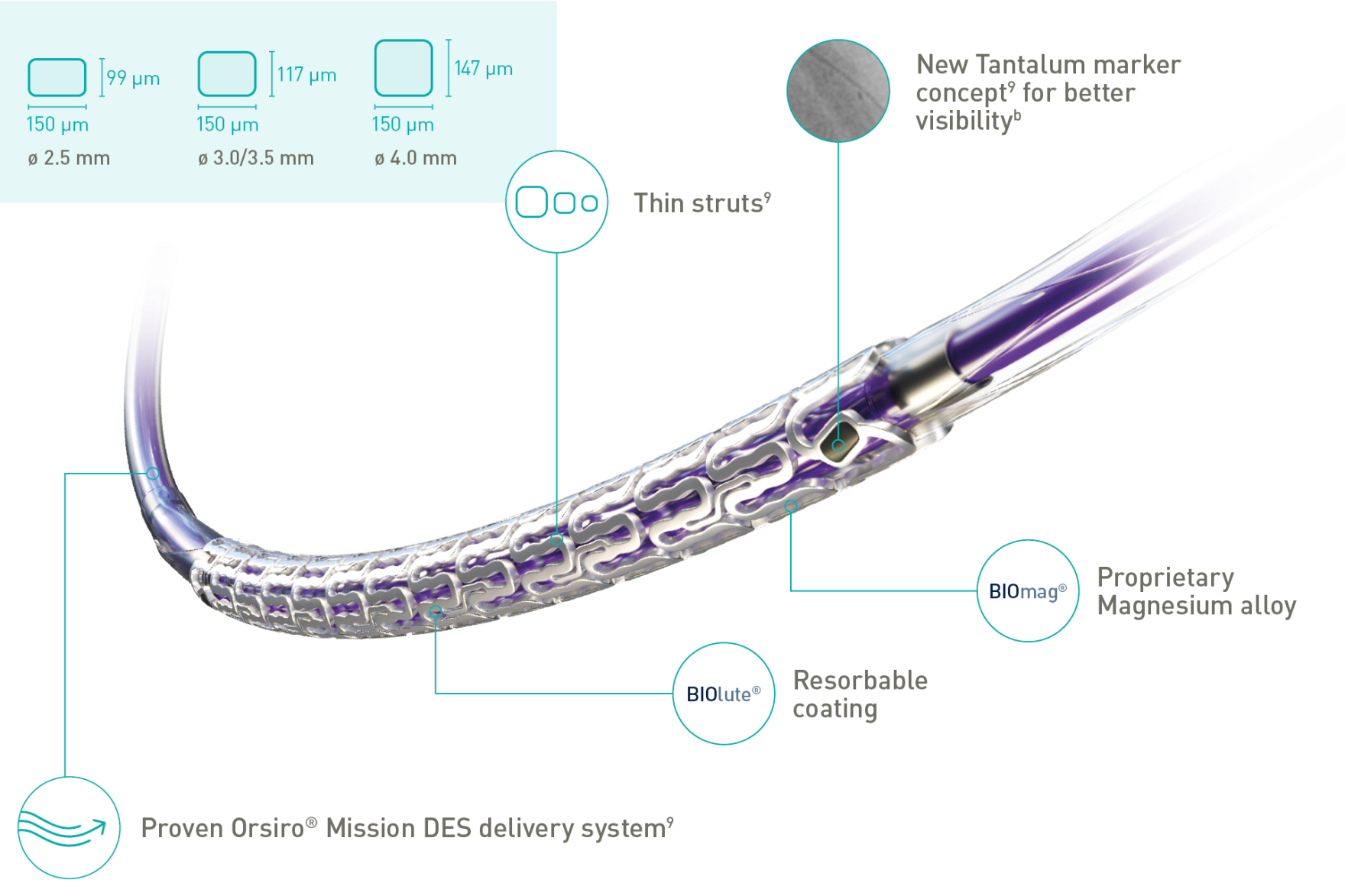
Freesolveᵀᴹ

Neuer Tantalmarker für bessere Sichtbarkeit
Dünne Streben
Resorbierbare Beschichtung BIOlute®
Unternehmenseigene Magnesiumlegierung BIOmag®
Technische Daten
| Scaffold | |||||
|---|---|---|---|---|---|
| Scaffoldmaterial | Unternehmenseigene Magnesiumlegierung BIOmag® | ||||
| Strebendicke | ø 2,5 mm: 99 μm; ø 3,0/3,5 mm: 117 μm; ø 4,0 mm: 147 μm |
||||
| Durchmesser bei maximaler Aufdehnung | Nenndurchmesser + 0,6 mm | ||||
| Marker | Ein ovaler Tantalmarker an jedem Ende | ||||
| Medikamentbeschichtung | BIOlute® bioresorbierbare Poly-L-Milchsäure (PLLA), die einen Limus-Wirkstoff freisetzt |
||||
| Einführsystem | |||||
| Kathetertyp | Rapid-Exchange | ||||
| Katheterlänge | 140 cm | ||||
| Empfohlener Führungskatheter | 6 F | ||||
| Crossing-Profil | ø 2,5 mm ≤ 1,3 mm; ø 3,0-4,0 mm ≤ 1,4 mm | ||||
| Führungsdraht-Durchmesser | 0,014” | ||||
| Nominaldruck (NP) | 10 atm | ||||
| Berstdruck (RBP) | 16 atm | ||||
Gefäßgröße
| Scaffold-ø (SD) (mm) |
Empfohlener ø (RVD) (mm) |
|---|---|
| 2,50 | 2,50 - 2,70 |
| 3,00 | 2,70 - 3,20 |
| 3,50 | 3,20 - 3,70 |
| 4,00 | 3,70 - 4,20 |
Compliance-Tabelle
| Balloon diameter (mm) | |||||
|---|---|---|---|---|---|
| ø 2,50 | ø 3,00 | ø 3,50 | |||
| Nominaldruck (NP) |
atm** ø (mm) |
10 2,52 |
10 3,04 |
10 3,54 |
|
| Berstdruck (RBP) |
atm** ø (mm) |
16 2,72 |
16 3,29 |
16 3,79 |
|
| *1 atm = 1,013 bar | |||||
Bestellinformationen
| Scaffold-ø (mm) |
Scaffoldlänge (mm) |
||||
|---|---|---|---|---|---|
| 13 | 18 | 22 | 26 | 30 | |
| 2,50 | 443103 | 443104 | 443105 | - | - |
| 3,00 | 443108 | 443109 | 443110 | 482156 | 443111 |
| 3,50 | 443113 | 443114 | 443115 | 482157 | 443116 |
| 4,00 | 443118 | 443119 | 443120 | 482158 | 443121 |
Downloads und weitere Links
Downloads
Weitere Links
Medien
Interviews mit Meinungsführern
Medien
Interviews mit Meinungsführern
Wie können wir Ihnen helfen?
Referenzen
Zielläsionsversagen (TLF) ist eine Kombination aus Zielgefäß-Myokardinfarkt (TV-MI), klinisch indizierter Revaskularisierung der Zielläsion (CD-TLR) und Herztod. *99,3 % sind nach 12 Monaten resorbiert (Marker sind nicht resorbierbar), basierend auf klinischen Daten; **Basierend auf Daten aus der quantitativen Koronarangiografie. a. Indikation gemäß Gebrauchsanweisung; b. BIOMAG-I-Fall bei normaler Projektion, mit freundlicher Genehmigung von Prof. Michael Haude, Rheinland Klinikum Neuss GmbH, Lukaskrankenhaus, Neuss, Deutschland; c. Xience Sierra DES (Abbott); d. Analyse von angiografischen Daten sowie von Daten aus der optischen Kohärenztomografie (OCT) zwei verschiedener BIOMAG-I-Fälle, mit freundlicher Genehmigung von Prof. Michael Haude, Rheinland Klinikum Neuss GmbH, Lukaskrankenhaus, Neuss, Deutschland; e. Das „4-P“-Protokoll wurde eingehalten.
1. IIB-Benchtest-Daten, BIOTRONIK Daten im Archiv. 2. Haude M. et al., The Lancet eClinicalMedicine 2023;59: 101940. 3. Haude, M. et al., EuroIntervention 2023;19:1-1, Online-Veröffentlichung im Mai 2023. 4. Seguchi M et al. OCT-Analyse 12 M., vorgestellt auf dem ESC 2023. 5. BIOTRONIK Daten im Archiv, Daten aus Benchtest IIB: Freesolve im Vergleich zu BIOTRONIK Orsiro Mission und Abbott Xience Sierra. 6. Basierend auf präklinischen Daten, Seguchi, M. et al., EuroIntervention 2023;18, Online-Veröffentlichung vor Druck, Januar 2023. 7. BIOTRONIK Daten im Archiv, im Vergleich zum Vorgängerprodukt. 8. Basierend auf der Analyse intravaskulärer OCT-Daten aus der BIOMAG-I-Studie, vorgestellt von Dr. M. Seguchi auf dem ESC 2023. 9. BIOTRONIK Daten im Archiv. 10. Byrne, RA. et al., Eur Heart J 2015;36:2608-2620. 11. Haude M., et al. Sustained safety and performance of the second-generation drug-eluting absorbable metal scaffold in patients with de novo coronary lesions: 12-month clinical results and angiographic findings of the BIOSOLVE-II first-in-man trial. Eur Heart J. 2016;37:2701-9.
BIOSOLVE-II und BIOMAG-I beruhen auf einer Kaplan-Meier-Analyse zur Fehlerschätzung.
BIOlute, BIOmag, BIOMAG, BIOSOLVE, Orsiro, Orsiro Mission, Magmaris und Freesolve sind Marken oder eingetragene Marken der Unternehmensgruppe BIOTRONIK. Alle anderen Marken sind Eigentum ihrer jeweiligen Inhaber.